Pianificazione chirurgica 3D: filo conduttore tra fase conoscitiva e virtuosismo tecnico clinico.
Medicina e tecnologia sembrano due temi che viaggiano in sinergismo, quasi come voler trovare gli uni negli altri lo scopo della loro esistenza. Le innovazioni tecnologiche in medicina stanno evolvendo a passo con i tempi , ma non con lo stessa rapidità la loro diffusione fa capolinea al beneficio del paziente, per i costi e per la facilita di impiego. La curva di apprendimento dei sistemi tecnologici è influenzata da numerosi fattori; in primo luogo l’evoluzione, si scontra con l’apprendimento delle generazioni mediche precedenti, le quali non hanno avuto imposto i ritmi di crescita, rispetto alle nuove generazioni. I giovani medici tra l’altro anche se informatizzati al punto giusto, si trovano a dover affrontare, crisi permettendo, la preparazione alle innovazioni stesse, le quali viaggiano su veicoli più veloci e costruiti spesso in paesi extraeuropei dove la crisi non fa da padrona.
Ma se entriamo nel vortice di tutte le tendenze in tema di evoluzione, ci accorgeremo che il comune denominatore, è la diffusione capillare, ovvero cercare di arrivare a più persone possibili con riduzione dei costi, e cosi come è successo per la tecnologia touch, tv smart, anche il 3D Printing ne sta seguendo le orme. Ben presto chiunque potrà acquistare e diventare produttore di qualsiasi cosa, a vantaggio di tutti. Gli effetti di questa nuova rivoluzione non sono ancora calcolabili ma fanno sicuramente rumors alcune notizie in merito, eccone un esempio:
Il primo rene da stampante 3d, modello per intervento d’organo quanto mai realistico è frutto del lavoro di un gruppo di chirurghi dell’università di Kobe, in Giappone. Il modello è stato realizzato come guida per preparare un intervento di asportazione di un tumore. Il cancro del rene è l’ottava neoplasia per diffusione, rappresenta il 3% di tutti i casi in Europa. Viene trattato chirurgicamente, ma l’intervento, che richiede precisione e velocità, può essere stressante per chi lo esegue. Da qui l’idea di realizzare un modello, più realistico possibile, di rene ‘malato’, ottenuto dai giapponesi combinando la capacità di imaging 3D della Tac con le nuove stampanti tridimensionali. Il risultato è stato un modello delle dimensioni esatte dell’organo reale, su cui i chirurghi si sono esercitati prima di asportare il difficile tumore renale.
L’utilizzo della tecnica, permette di ottenere un modello personalizzato, stampa del organo del paziente che nel nostro caso saranno le ossa mascellari. Avremo così la possibilità di esercitarci per l’intervento preventivamente, così; anche i più giovani chirurghi affronterebbero l’intervento reale in maniera più preparata.
La stampa 3D è un concetto abbastanza semplice. Si scarica un file digitale, che riguarda la “mappa” dell’oggetto da stampare, nel nostro caso un file radiografico stl e la macchina fa il resto. La stampante legge i file e produce l’oggetto realizzando strato su strato in materiale plastico specializzato. Poco tempo e l’oggetto del desiderio è pronto e “self-made”.
Una vera e propria rivoluzione 3D è quindi in corso.
(The Economist, in un editoriale del 10 febbraio 2011) così afferma:
« La stampa tridimensionale rende economico creare singoli oggetti tanto quanto crearne migliaia e quindi mina le economie di scala. Essa potrebbe avere sul mondo un impatto così profondo come lo ebbe l’avvento della fabbrica… Proprio come nessuno avrebbe potuto predire l’impatto del motore a vapore nel 1750 — o della macchina da stampa nel 1450, o del transistor nel 1950 — è impossibile prevedere l’impatto a lungo termine della stampa 3D. Ma la tecnologia sta arrivando, ed è probabile che sovverta ogni campo che tocchi. »
Sembra chiaro quindi, che un cambiamento radicale nel mondo tecnologico così importante coinvolgesse anche il nostro settore con effetti sull’economia non ancora valutabili. Ciò che va fatto a mio avviso, nel cambiamento a cui assistiamo e nell’attesa di un assestamento, è cercare di applicare le conoscenze già a noi note ad i nuovi input provenienti dal mercato, attuando cambiamenti significativi alle nostre tecniche.
Sfruttando questa semplice tecnologia potremmo:
-Entrare a far parte della rivoluzione di stampa 3D, per il beneficio del paziente.
-Contenere i costi della terapia senza rinunciare elle innovazioni tecnologiche.
-Rendere chiari i punti della terapia, dalla fase diagnostica interpretativa, alla fase clinica operativa.
-Migliorare l’approccio comunicativo, attraverso i mezzi virtuali e reali con il paziente.
-Dare maggiore predicibilità ai nostri trattamenti.
Il corso che ci proponiamo di offrire, ha come scopo il miglioramento della gestione chirurgica, dalla fase diagnostica iniziale alla fase operativa finale, nei casi semplici e complessi
Mediante l’utilizzo di modellini 3d dei mascellari ricavati da un semplice file stl e mediante l’utilizzo di stampanti 3d, si potrà pianificare realmente, l’inserimento di impianti, effettuato, secondo il dato protesico precedentemente maturato su modello in gesso.
La pianificazione implantare, protesicamente guidata, verrà effettuata in maniera reale, sulla replica ricavata con tecnica 3D printing del segmento osseo del paziente come se fosse un vero intervento.
L’inserimento ci permetterà di prevedere con una precisione approssimativa nell’ordine di 0.2 mm la presenza o meno di eventuali difetti ossei, causa di deiscenze o fenestrazioni al piano implantare. La conoscenza anticipata ed apprezzata realmente nelle proprie mani permetterà di poter quindi intervenire sul modellino per l’eventuale tecnica rigenerativa più appropriata:
Finalità ed obiettivi.
1) Scegliere la dimensione e la forma più appropriata delle griglie e membrane per il miglior supporto e l’eventuale GBR.
2)Scegliere la giusta quantità e volumetria dei materiali scaffold.
3) Modellare in anticipo le griglie al modello con i relativi punti di ancoraggio per la stabilità, quindi scegliere in maniera serena tra le tecniche rigenerative, quella più adatta ed a maggiore predicibilità.
4) infine, la posizione degli impianti al modello permetterà di estrapolare nel proprio laboratorio una guida per l’eventuale trasferimento dei dati nel cavo orale al momento dell’intervento.
Cosa si ottiene dal corso?
Questa tecnica permetterà di poter affrontare i propri interventi in assoluta serenità sia dal punto di vista medico legale, ma soprattutto dal punto di vista clinico chirurgico sicuri di poter affrontare gli interventi in assoluta predicibilità su tutti i possibili rischi e complicanze del caso. La pianicazione cosi effettuata, avrà dei costi contenuti e potrà essere affrontata con mezzi semplici, sfruttando di tutta la tecnologia del momento con le stampanti 3d in commercio (dal virtuale 3d al modello reale 3d).
1° caso clinico descrittivo.
Anche per questo caso, la chiave di volta del piano di cura appare quindi essere la messa a punto di un protocollo operativo volto a definire in modo chiaro un PIANO DI TRATTAMENTO RAZIONALE che si articola attraverso i seguenti punti:
1)Raccolta dei dati clinici e anamnestici.
2)Studio del caso: valutazione dei rischi e classificazione dei difetti in esame.
3)Analisi delle tecniche chirurgiche e dei rischi connessi al caso.
4)L’ipotesi del piano di trattamento razionale
5)La discussione attraverso il blog, del piano di trattamento ipotizzato
1. Raccolta dei dati clinici e anamnestici.
E’ giunto alla nostra osservazione un paziente di anni 40 in buone condizioni di salute generale, che riferiva assenza di farmaco-allergie con profilo di rischio medico generico da noi classificato come ASA1. Il paziente riferiva di una storia clinica di ricorrenti fenomeni ascessuali, successivi a terapie per il recupero endodontico e protesico degli elementi in sede 4.6;4.7. Tali elementi furono estratti sei mesi or sono, in seguito a frattura della porzione ceramica dell’elelemto protesico e contemporanea complicanza endodontica.
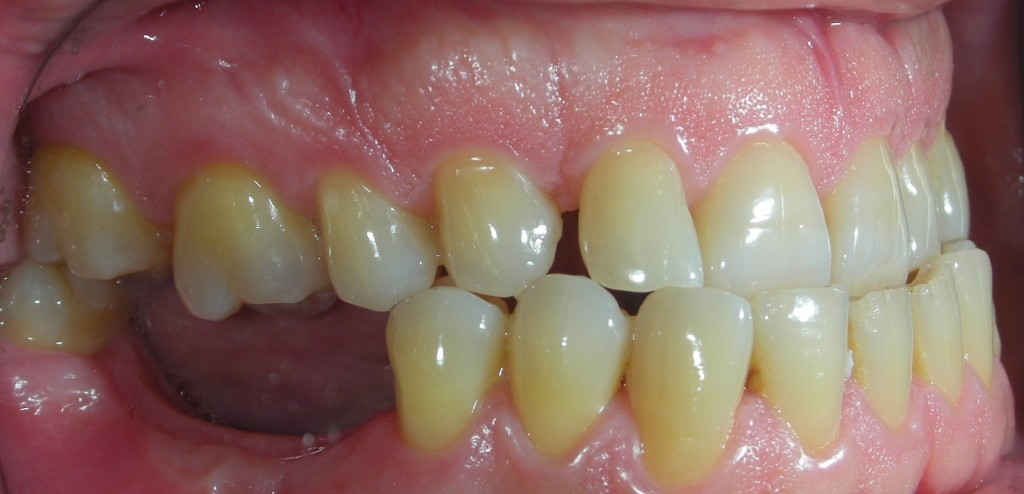
L’esame obiettivo intra- ed extra- orale mette in evidenza la presenza di un’occlusione di terza classe con inversione anteriore del morso e cross bite bilaterali, l’assenza di neoformazioni palpabili, la presenza di cute e mucose normoemiche con lingua in asse e normomobile, frenuli correttamente inseriti, livello di attacco clinico gengivale nei limiti della norma, assenza di processi cariosi in atto, lieve estrusione del 1.6, inclusione de 1.3. Il paziente non presenta abitudini viziate, e parafunzioni, non fumatore. L’esame occlusale non mette in evidenza alterazioni a carico dell’ A.T.M.
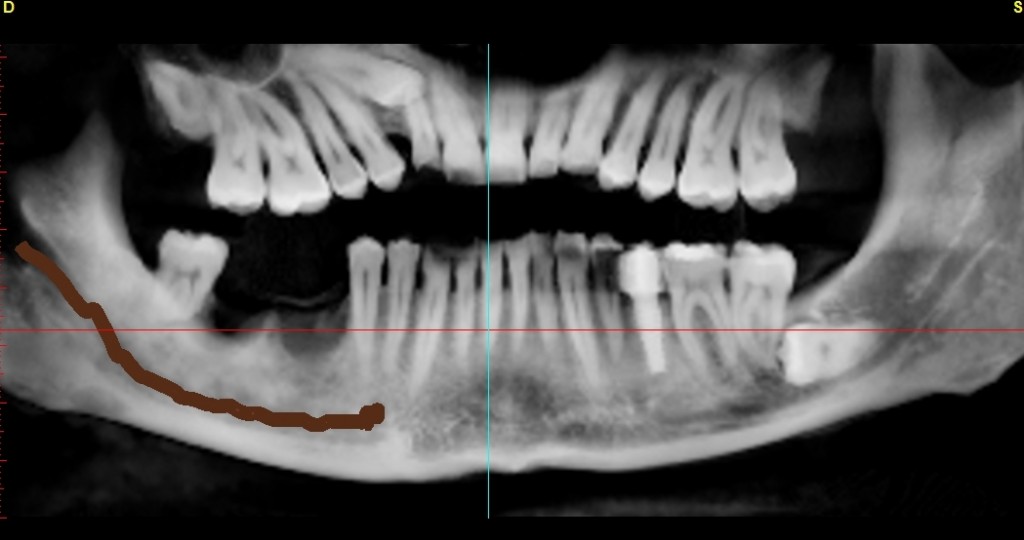
È evidente edentulia in sede 4.6;4.7 con associato un difetto osseo verticale ed orizzontale il quale richiede una attenta valutazione pre chirurgica.
Fig. 1.1; 1.2; 1.3
Fig 1: Visione frontale.
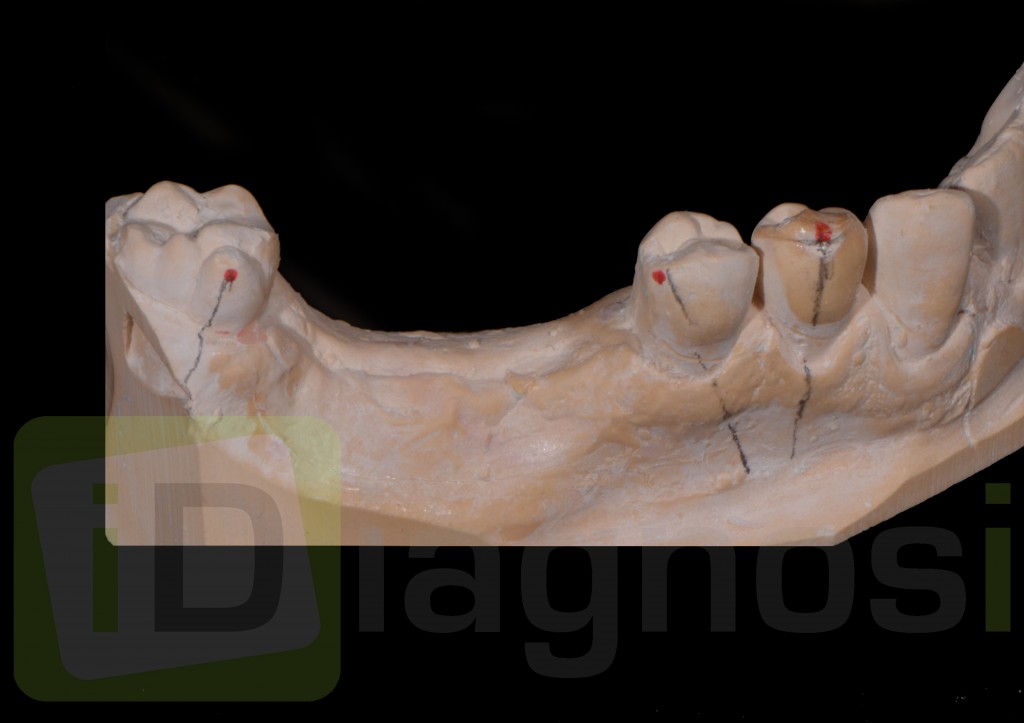
Fig 2: vista laterale edentulia in sede 4.6;4.7 con associato ampio difetto osseo verticale.
fig 3: difetto osseo orizzontale.
2. Studio del caso: valutazione dei rischi e classificazione dei difetti in esame
Ai fini di un eccellente fase di painificazione occorre valutare, la presenza dei fattori di rischio locali dai quali spesso dipendono i fallimenti precoci e tardivi.
I fattori di rischio da valutare sono:
A. Rischio estetico.
B. Rischio biomeccanico.
C. Rischio infiammatorio-infettivo.
D. Rischio legati al sito edentulo.
A. Rischio estetico.
Anche se gli elementi in questione non sono considerati elementi di importanza ai fini estetici, c’è comunque da considerare che una corretta emergenza dei tessuti molli, (intesa come qualità e spessore della gengiva aderente), sarebbe in grado sia di donare maggiore naturalezza agli elementi, ma sopratutto rappresenterebbe una condizione favorevole al mantenimento igienico delle prime spire degli impianti.
B. Rischio biomeccanico
Il rischio biomeccanico è un fattore di fondamentale importanza per il successo implantare a breve e a lungo termine. Le forze applicate al sistema stomatognatico vanno attentamente valutate al fine di intercettare e quindi eliminare ogni potenziale fonte di sovraccarico funzionale che comprometterebbe la terapia già nell’immediato post-chirurgico, inficiando l’osteointegrazione implantare. E’ da tenere ben presente, la terza classe molare, il morso inverso, il cross bite e estrusione del 1.6.
C. Rischio infiammatorio infettivo.
L’esame obiettivo non ha rilevato segni di gengivite. Il paziente presenta un buon controllo della placca batterica, non sono evidenti agli esami strumentali, compromissioni del parodonto profondo. Non si rivela la presenza, in vicinanza del sito d’interesse, di possibili fonti infettive quali lesioni cariose in atto o trattamenti endodontici incongrui.
D. Rischi legati al sito edentulo.
L’attenta valutazione qualitativa e quantitativa del sito ci permette di classificarne la morfologia, facilitando la fase diagnostica pre-chirurgica e sopratutto ci da la possibilità di mettere a confronto tra le diverse tecniche chirurgiche da poter eseguire, quella a minor rischio e con maggiore predicibilità a lungo termine.
Dallo sviluppo delle impronte, è possibile estrapolare una serie di dati che già lasciano intravedere la morfologia dell’atrofia ossea che sottende l’edentulia (fig. 2.1).
fig 2.1
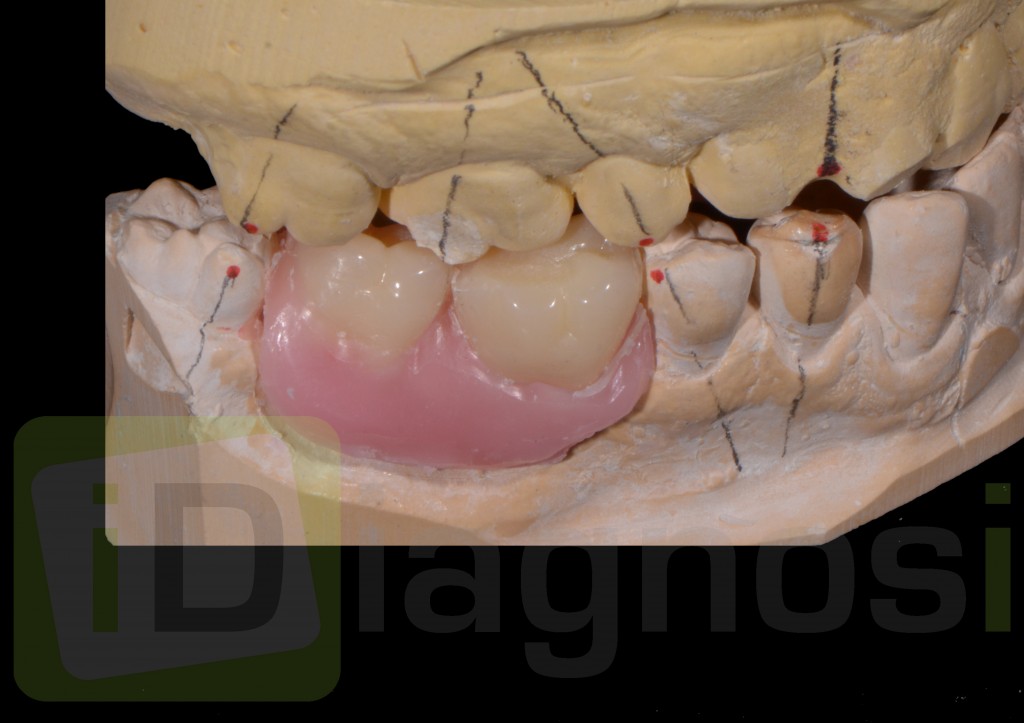
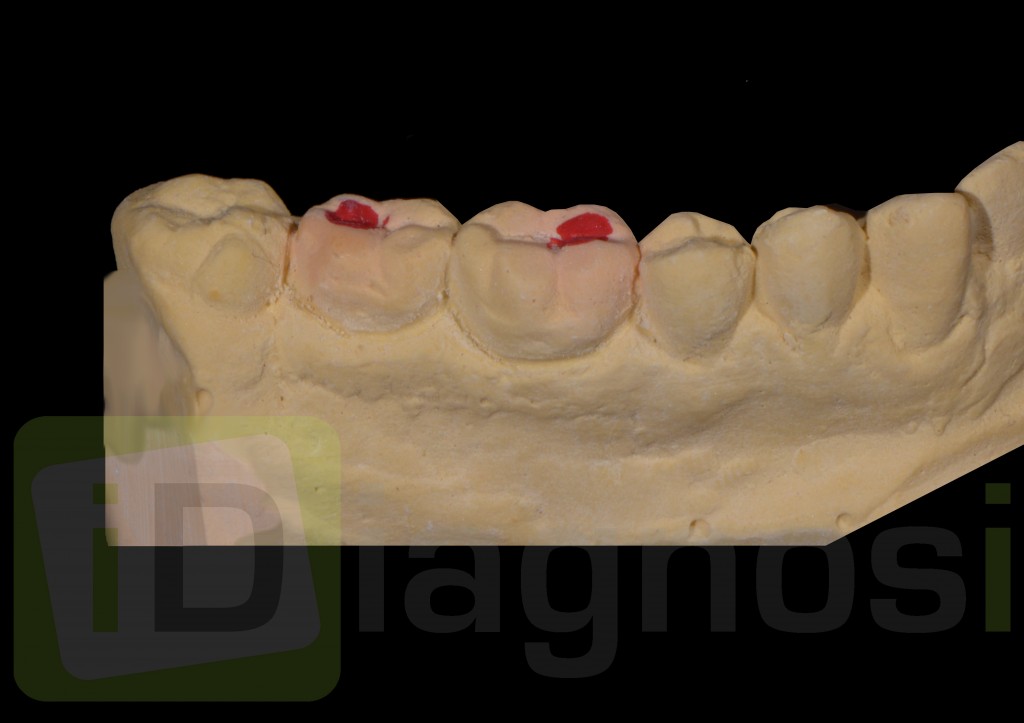
Il montaggio ideale protesico degli elementi sul modello permette di conoscere quei valori numerici a cui fare riferimento per la nostra pianificazione. Il riempimento con cera rosa permette di valutare preliminarmente il difetto osseo verticale crateriforme, ed orizzontale di 6 mm. (fig. 2.2). E la necessita di intrusione dell’elemento 1.6 estruso.
fig 2.2
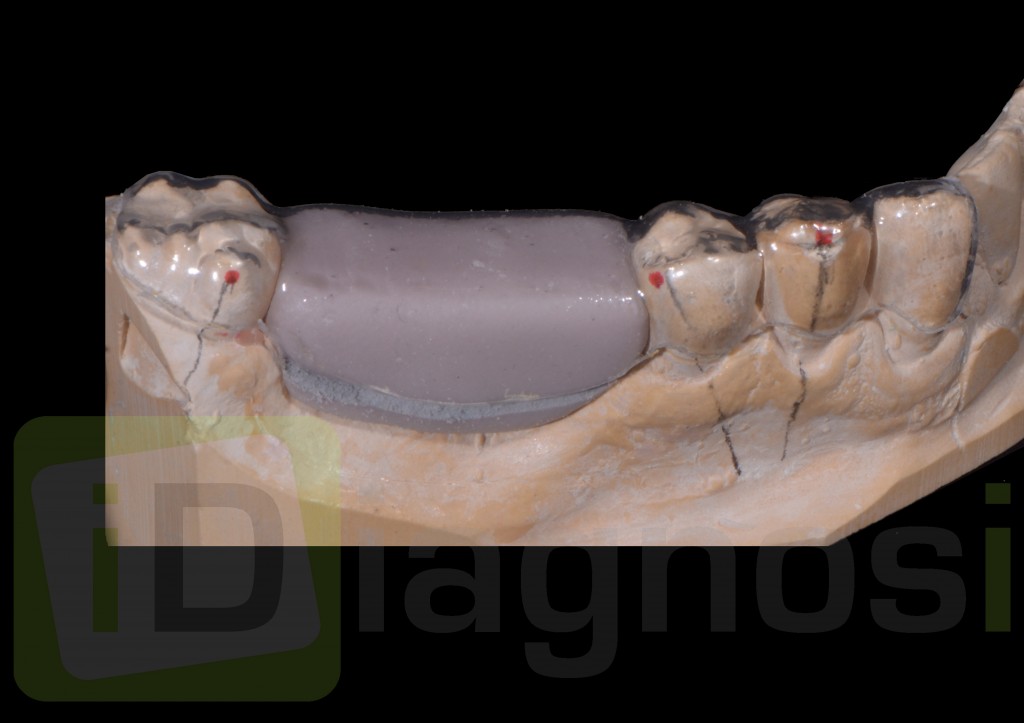
Gli spazi protesici indicano per il rispetto delle armonie spaziali degli elementi adiacenti, la presenza di uno spazio adeguato alla riabilitazione, nella porzione coronale, a livello crestale, è invece presente un’eccesso di spazio mesio distale che andrà attentamente valutato ai fini della corretta scelta degli impianti da inserire. (Fig2.2).
fig 2.3
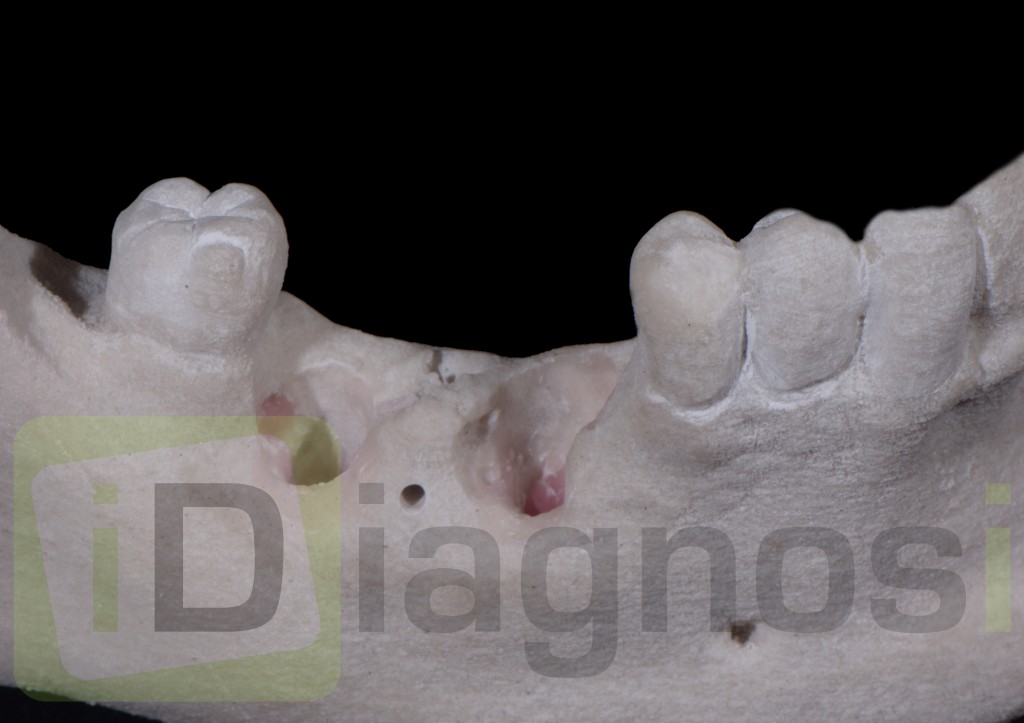
Il confronto tra il sito chirurgico ed il controlaterale sano, permette di valutarne le condizioni, rappresentate da;
1) Ampio deficit osseo verticale.
2) Ridotto spessore osseo vestibolare,di circa 6 mm.
Il caso in esame presenta quindi alti fattori di rischio biomeccanico, legate all’estrusione del 1.6. Il sito edentulo viene classificato come (IV classe di Cawood ed Howell), dove l’atrofia della porzione vestibolare richiede un mamgement dei tessuti molli adeguato nella scelta del disegno del lembo in previsione dell’ipotetico allungamento dello stesso, richiesto per far fronte al grado di atrofia seppur minima della cortex alveolare vestibolare. Le difficoltà nella scelta del piano di trattamento più adeguato sono inoltre legate alla scelta del diametro degli impianti da Inserire e della tecnica rigenerativa più appropriata.
3. Analisi delle possibili tecniche chirurgiche e dei rischi connessi al caso.
Attraverso l’adozione consapevole di un sistema di dubbio e dell’incertezza, o meglio della probbabilità della certezza, cercheremo di adottare le decisioni più appropriate per il nostro percorso diagnostico razionale.
I dubbi e le domande che dovremmo farci saranno:
A. quanti e quali impianti inserire?
B. quale tipo di lembo?
C. quali materiali?
D. occorrono ulteriori indagini?
A. Quanti e quali impianti inserire?
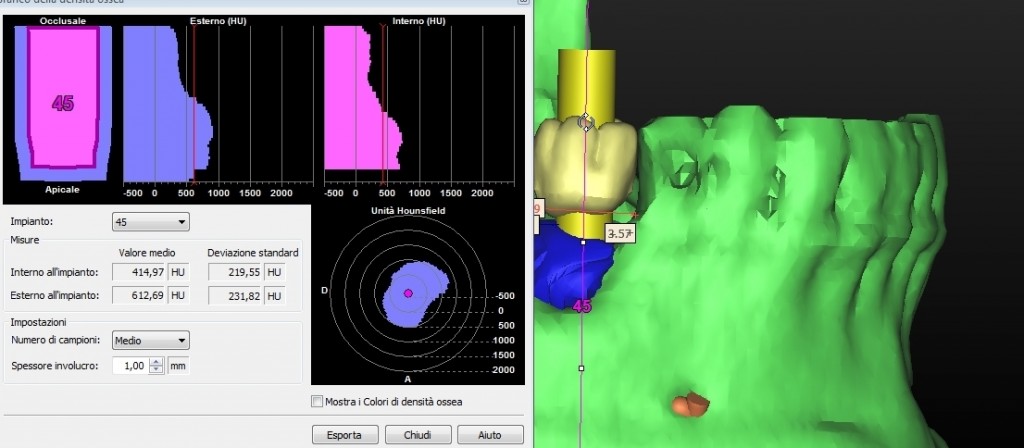
Grazie ai software di pianificazione è stato possibile prevedere con precisione dettagliata, gli obiettivi della pianificazione chirurgica implantare, scegliere quindi, con previsione protesica soddisfacente la lunghezza il diametro degli impianti da inserire.
Fig 3.4: visione Rx panoramica: evidente difetto osseo.
Fig 3.5: pianificazione virtuale rigenerativa ed implantare.
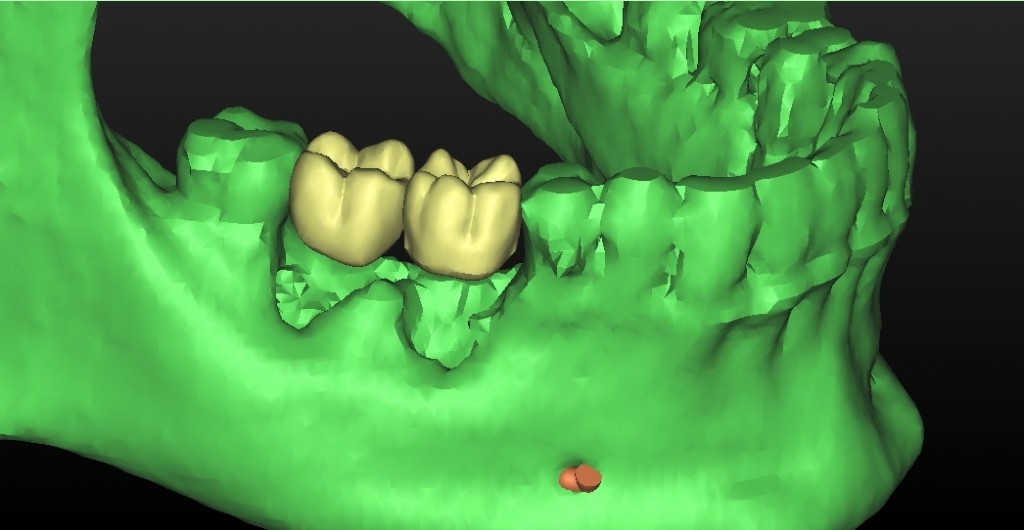
Fig 3.6: modello virtuale 3D con evidente difetto osseo.
Fig 3.7: ricostruzione degli elementi dentari.
Fig 3.8: Ricostruzione virtuale del difetto osseo.
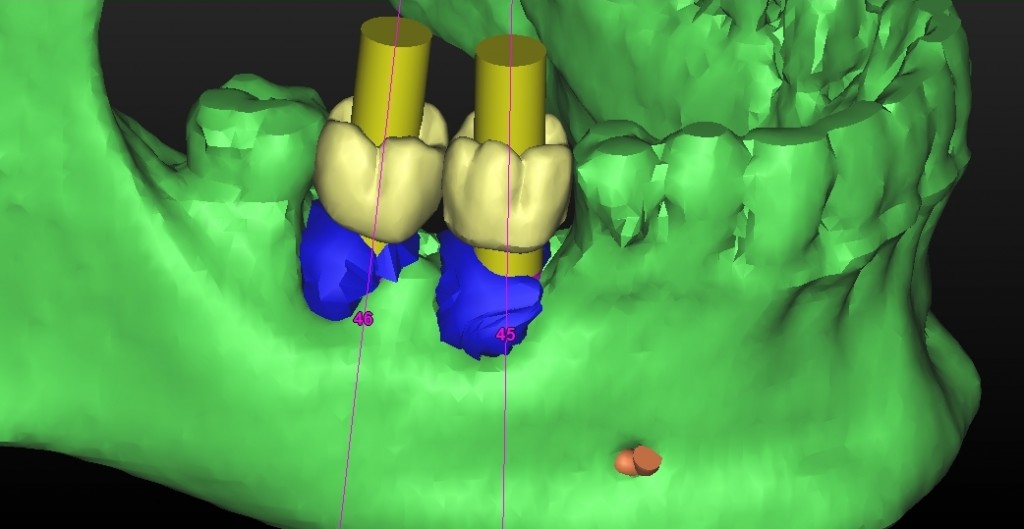
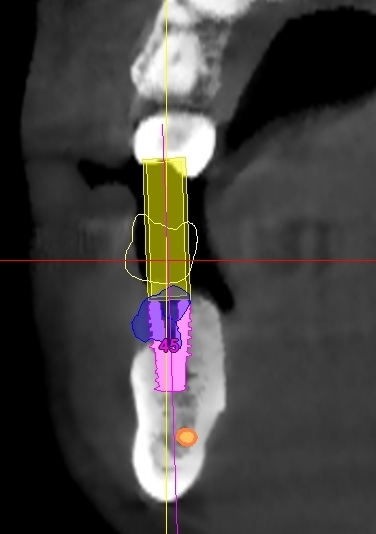
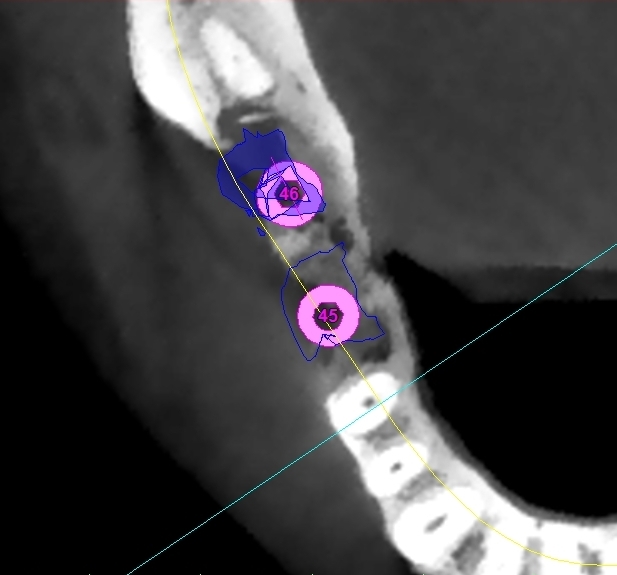
Fig 3.9: pianificazione implantare.
Fig 3.10: pianificazione implantare.
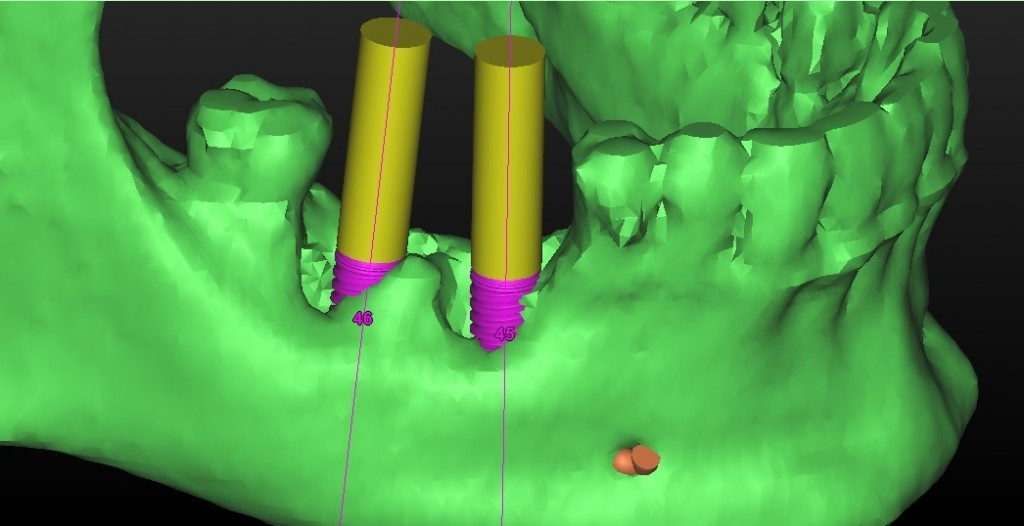
Fig 3.11: pianificazione implantare.
Fig 3.12: pianificazione implantare.
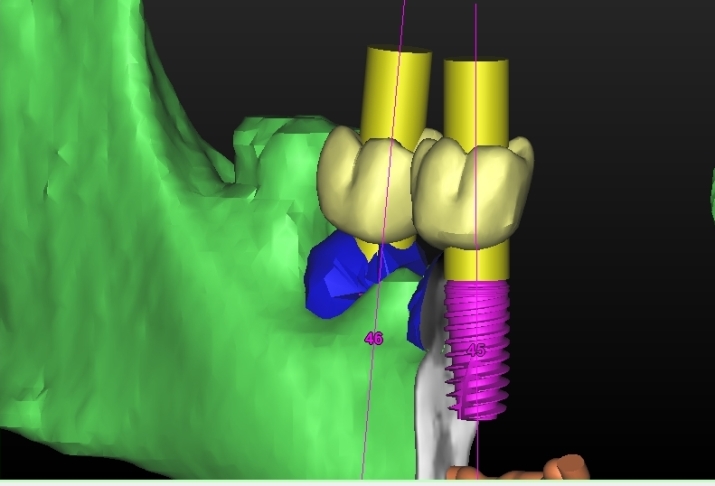
Fig 3.13: pianificazione implantare.
Fig 3.14 pianificazione implantare.
Fig 3.15 pianificazione implantare.
Fig 3.16
Fig 3.17
Fig 3.18
FiG 3.19
Fig 3.20
B. Quale tipo di lembo?
Le incisioni e il lembo da eseguire dovrebbero permetterci di gestire i tessuti molli nella maniera tale da:
1) Accedere in maniera generosa all’area dell’intervento.
2) Permettere un prelievo dal piatto corticale mandibolare.
3) Poter determinare un’allungamento dei tessuti per far fronte all richiesta di volume indotta dal riempimento di materile osseo prelevato.
4) chiudere per prima intenzione il lembo principale.
Un lembo a cui potremmo far riferimento è la tecnica della periostioplastica, descritta dettagliatamente dall’autore (Prof. Mauro Merli, in terapia implantare, il piano di trattamento integrato; cap. 11 quintessenza ed.). Questa tecnica permette di ottenere attraverso delle incisioni periostali, eseguite nello spessore del lembo principale, nel limite del periostio, un doppio strato tissutale, grazie al quale viene facilitata la fase di chiusura del lembo principale favorendo un perfetto sigillo della linea di incisione e del materiale da rigenerazione, permetterebbe inoltre l’aumento del tessuto molle per effetto di sovrapposizione del doppio tessuto.
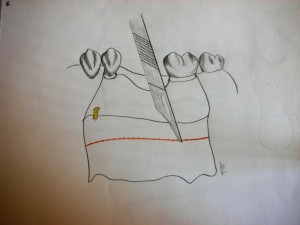
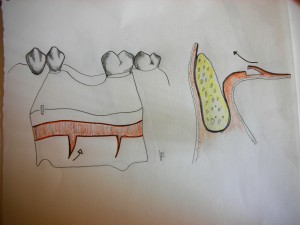
La tecnica di base prevede di scolpire e sollevare dapprima un lembo mucoperiostale trapezoidale, verrà eseguito quindi l’inserimento degli impianti ed eseguita la ricostruzione ossea e solo dopo aver posizionato la membrana di ricopertura, verrà eseguita un’incisione orizontale di rilascio, seguita da due incisioni verticali che coinvolgono lo spessore dello stato periostale all’interno del lembo mucoperiosteo stesso. Il lembo periostale, verrà quindi ribaltato e suturato con suture riassorbilbili al lembo linguale costituendo il primo sigillo di chiusura. Verrà poi suturato il lembo principale trapezoidale con suture ad u orizontale e punti staccati in corrispondenza dell’incisione primaria linguale. Un’esempio è riportato nelle immagine dei disegni (fig. 3.21;3.22;3.23)
fig 3.21 incisione periostale primaria orizzontale.
fig 3.22 allungamento del lembo principale, sull’incisione periostale.
fig 3.23 incisioni periostali verticali di rilascio.
Facendo ricorso a questa tecnica dovremmo riuscire ad ottenere una chiusura per prima intenzione del lembo, in assenza di tensioni, riducendo il rischio di deiscenza e contemporanemente aumentare il volume dei tessuti molli nell’area di innesto.
C. Quali materiali?
In questo caso il tipo di difetto consente di inserire gli impianti contestualmente alla rigenerativa della corticale vestibolare. Il materiale da considerare è sicuramente il gold standard ovverro l’osso autologo, prelevato mediante tecnica di bone scraper, per l’apporto osteoinduttivo, miscelato a osso eterologo e protetto mediante una griglia rigida e membrana riassorbile in collagene o pericardio.
I nostri obiettivi sono allora ben delineati, cioè quelli di inserire due impianti in un solo tempo chirurgico, riportare il nostro difetto di classe IV a classe III di Cawood ed Howell, attraverso il prelievo di particolato osseo vicino alla sede di nostro interesse per la correzione morfologica della atrofia ossea e ridurre così al minimo i rischi intrinseci chirurgici.
D. occorrono ulteriori indagini ?
A questo punto della pianificazione, avere a disposizione la replica del segmento osseo del paziente ci consente di ottenere una serie di informazioni reali alle quali potremmo avere accesso solo in fase chirurgica. Spesso ci confrontiamo con interventi complessi durante i quali il fattore tempo, ci influenza e diventa fondamentale, durante, dover gestire una serie di scelte, che nel nostro caso effettueremo prima in assoluta serenità, dando più valore all’esercizio chirurgico il quale verrà migliorato durante l’intervento reale.
Fig 3.24 modello in gesso preliminare.
Fig 3.25 montaggio in cera.
Fig 3.26 replica in gesso.
Fig 3.27 realizzazione della mascherina termostampata.
Fig.3.27 realizzazione della mascherina termostampata.
fig: modello 3D preliminare.
Fig 3.28: Sulla scorta della informazioni del piano implantare, ottenute dal modello virtuale, ma soprattutto dall’assoluta tranquillità di operare su un modello con rapporto 1/1 eseguiamo le stesse sequenze osteotomiche fino all’inserimento degli impianti nel modello 3D.
Fig 3.29 impianti analoghi replica inseriti.
Fig 3.30 ricostruzione del difetto osseo mediante silicone trasparente.
fig…. scelta della griglia più idonea in base al difetto.
Fig 3.31 modellazione della griglia e delle viti di osteosintesi ai punti di ancoraggio sull’osso residuo.
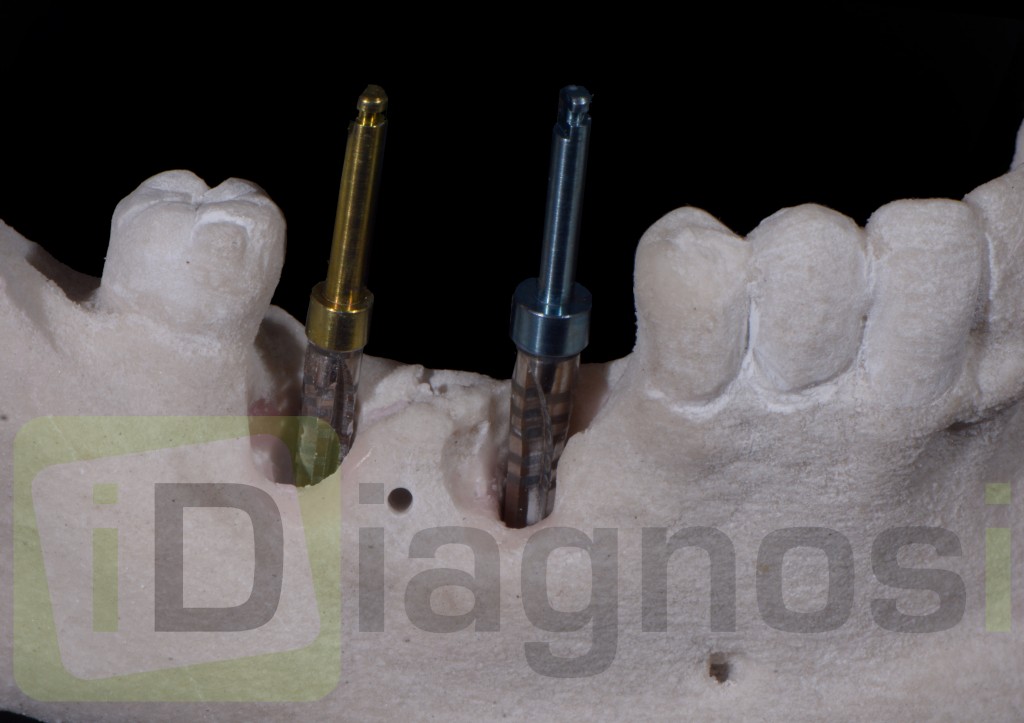
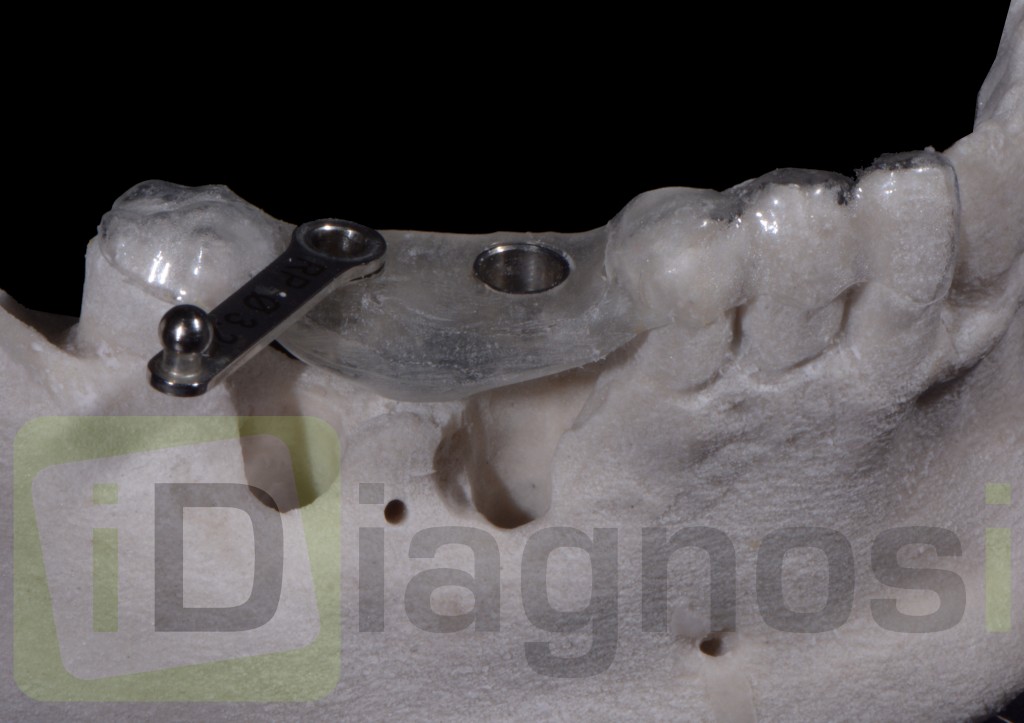
Fig 3.32 realizzazione della mascherina di guida osteotomica: montaggio della sleeve e vite guida.
Fig 3.33
Fig.3.34
Fig. 3. 35
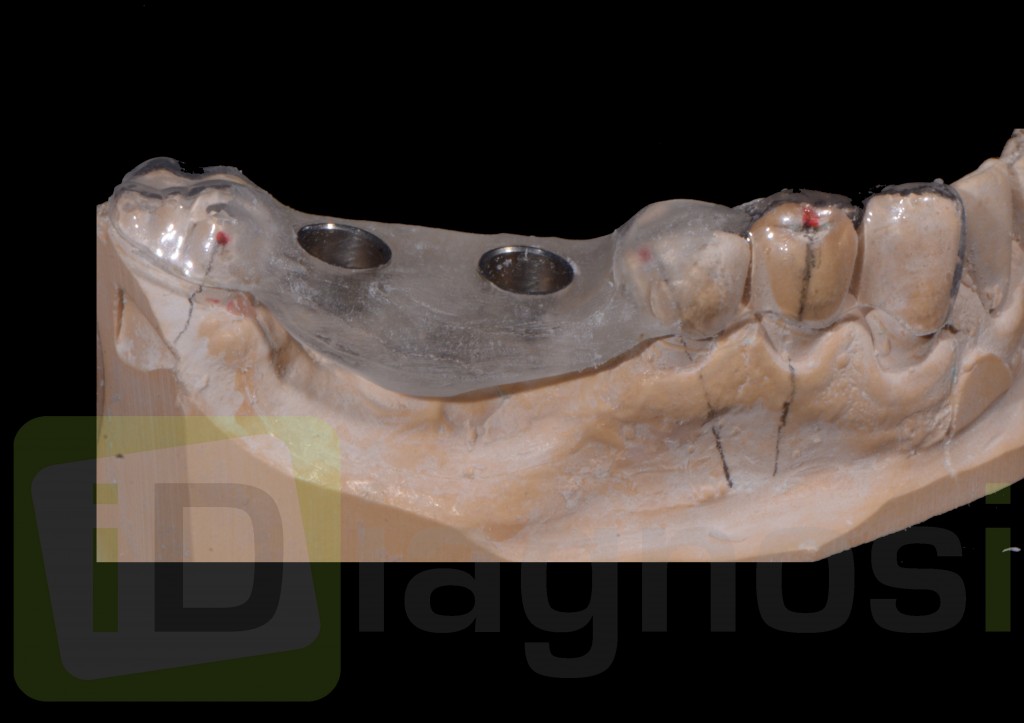
Fig. 3. 36 trasferimento della mascherina al modello stampa 3D.
Fig.3.37 trasferimento alla mascherina.
Fig.3.38 trasferimento alla mascherina.
Fig.3.39 trasferimento alla mascherina.
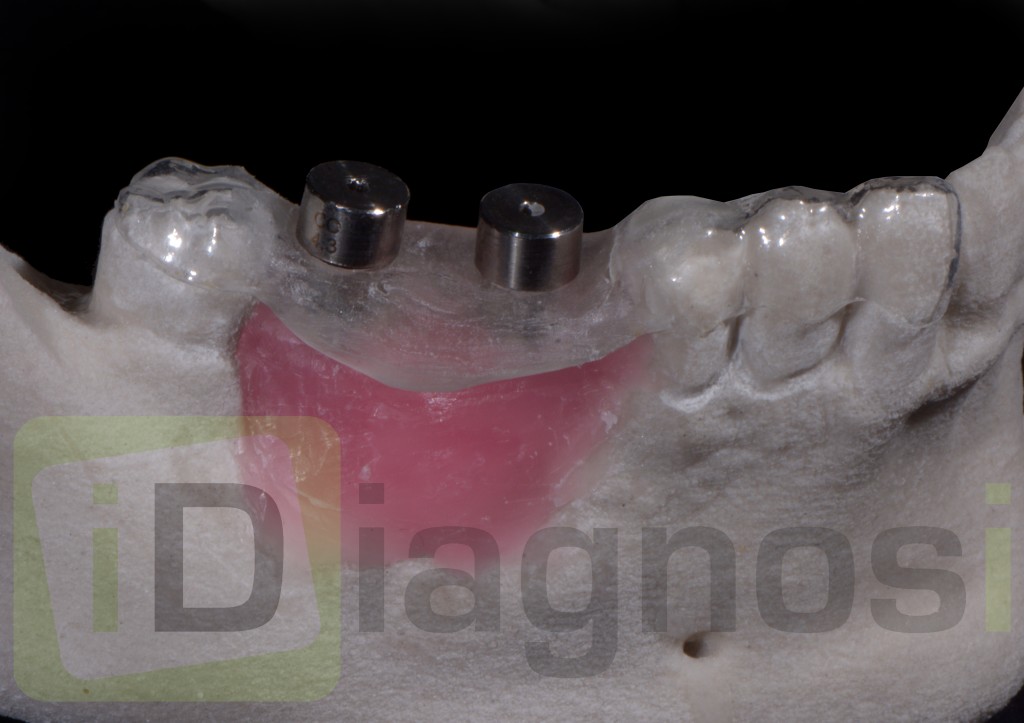
Fig.3.40 verifica della mascherina al modello in gesso.
Fig3.41
Fig3.42 prove delle frese per chirurgia guidata.
Fig.3.43 prove delle frese per chirurgia guidata.
Fig3.44 prove delle frese per chirurgia guidata.
3.45:mod. finale con materiale di riempimento del difetto.
Fig: 3.46 prova di corrispondenza della guida chirurgica.
Fig: 3.47 prova di corrispondenza della guida chirurgica.
4. L’ipotesi del piano di trattamento razionale
Divideremo per semplicità le nostre ipotesi del piano di trattamento in punti così da facilitare i visitatori del blog ad intervenire, suggerire, avanzare dubbi, così da ridurre ancora di più le nostre incertezze.
1) Utilizzo di colluttorio alla clorexidina al 0,2% per un minuto e infiltrazione di anestetico al sito chirurgico.
2) Anestesia plessica carbocaina al 2% con adrenalina
3) Apertura di un lembo mucoperiosteo trapezoidale con incisione mediocrestale, estensione intrasulculare mesiale all’elemento 4.5; estensione intrasulculare distale all’elemento 4.8. Incisione di scarico verticali mesiale al 4.5 e distale al 4.8 oltre la giunzione muco gengivale, con attenzione all’emergenza del nervo mentoniero sullo scarico mesiale.
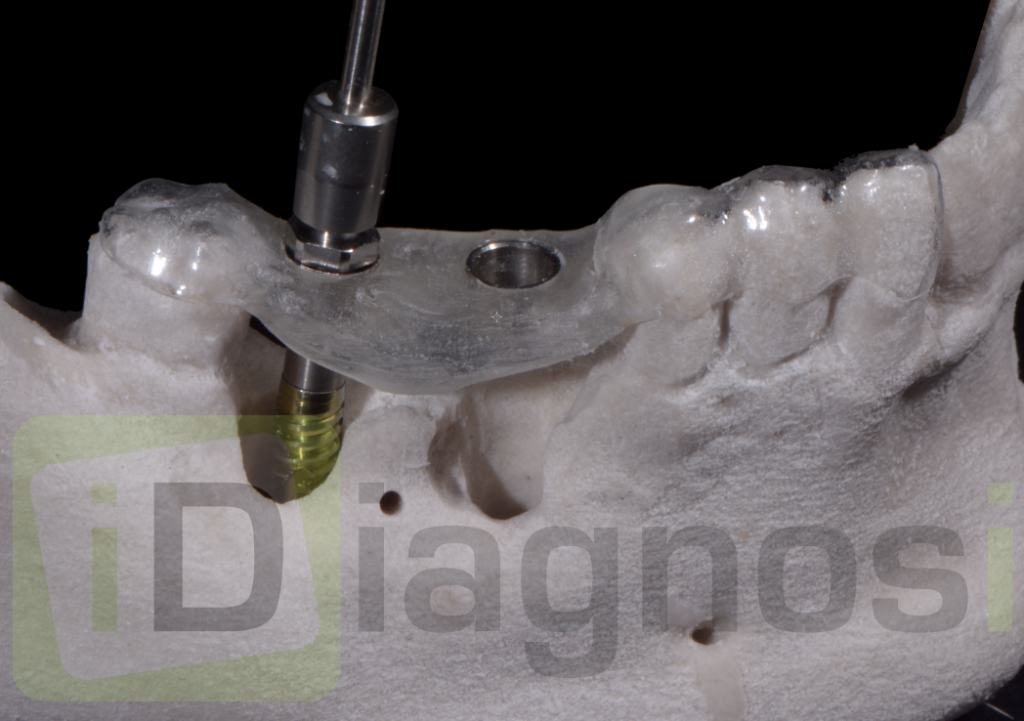
4) Preparazione dei siti osteotomici attraverso la guida chirurgica e frese calibrate di diametro 2;2.8;3.2 con lunghezza programmata a 23 mm.
5) Posizionamento degli impianti. 2 impianti 4.9/13 mm, Posizionare tamponi agli sbocchi ghiandolari
6) Prelievo dalla cortex mandibolare, del particolato, mediante tecnica bone scraper, miscelazione al 50% con granuli bio oss 1-2 mm e conservazione.
7) Incisione periostale orizzontale, di rilascio del lembo.
8) Incisioni verticali periostali di preparazione del lembo con tecnica della perioosteoplastica.
9) Preparazione del sito ricevente, apertura degli spazi midollari
10) Posizionamento del particolato, fissaggio della griglia metallica e protezione mediante membrana riassorbibile.
11) Sutura del doppio lembo mediante suture riassorbibili intramurali a materassaio orizzontale per il lembo periostale, e a punti staccati per il lembo principale mucoperiosteo.
Fase chirurgica:
Utilizzo di colluttorio alla clorexidina al 0,2% per un minuto e infiltrazione di anestetico al sito chirurgico. Anestesia plessica carbocaina al 2% con adrenalina
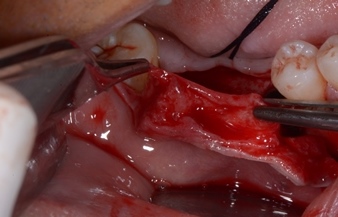
Apertura di un lembo mucoperiosteo trapezoidale con incisione mediocrestale, estensione intrasulculare mesiale all’elemento 4.5; estensione intrasulculare distale all’elemento 4.8. Incisione di scarico verticali mesiale al 4.5 e distale al 4.8 oltre la giunzione muco gengivale, con attenzione all’emergenza del nervo mentoniero sullo scarico mesiale.
Difetti ossei evidenti.
Prova della mascherina.
Preparazione dei siti osteotomici attraverso la guida chirurgica e frese calibrate di diametro 2;2.8;3.2 con lunghezza programmata a 23 mm.
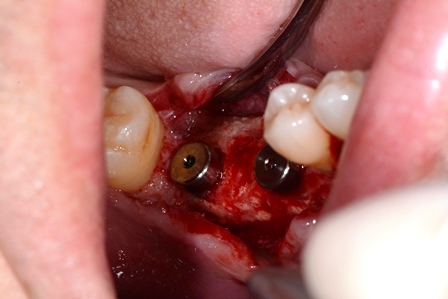
Posizionamento degli impianti. 2 impianti 4.9/13 mm.
Posizionare tamponi agli sbocchi ghiandolari
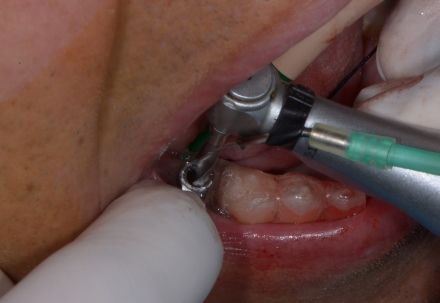
Prelievo dalla cortex mandibolare, del particolato autologo mediante tecnica bone scraper e conservazione.
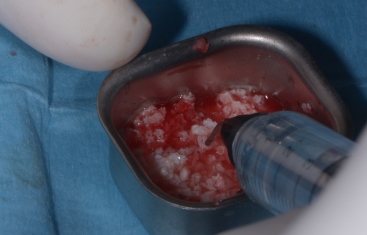
bone scraper e osso autologo.
Miscelazione al 50% con granuli bio oss 1-2 mm e conservazione.
Miscelazione al 50% con granuli bio oss 1-2 mm e conservazione.
idratazione del particolato con sangue e acqua fisiologica.
Incisione periostale orizzontale, di rilascio del lembo: tecnica della periostioplastica secondo Merli.
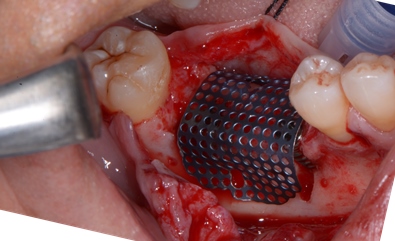
Prova della congruità della griglia precedentemente modellata su stampa 3d.
Apertura degli spazi midollari.
Riempimento dei difetti.
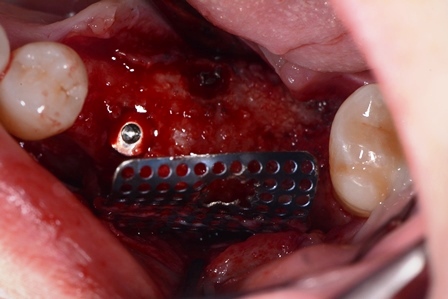
Fissaggio della griglia.
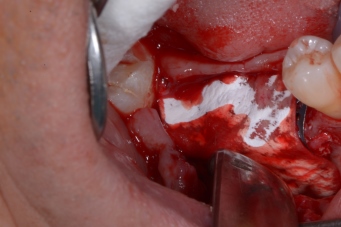
adattamento della membrana geisthlich bio guide
Chiusura per prima intenzione senza tensioni del lembo linguale con la plastica del lembo vestibolare mediante sutura in vicril 5 /0 a materassaio interno.
Sutura esterna doppia: materassaio esterno in seta. sutura continua in vicril, incisione di rilascio vestibolare in ptfe.
Controllo a 10 giorni e rimozione della suture.
Controllo a tre settimane dalla rimozione della suture.
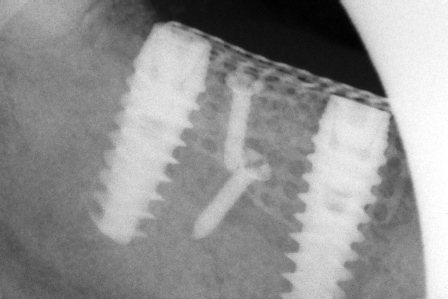
Rx endorale a 7 mesi dall’intervento
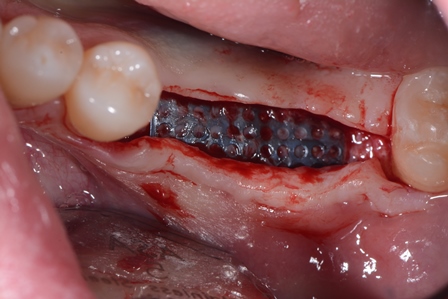
Riapertura del lembo e rimozione della griglia in titanio.
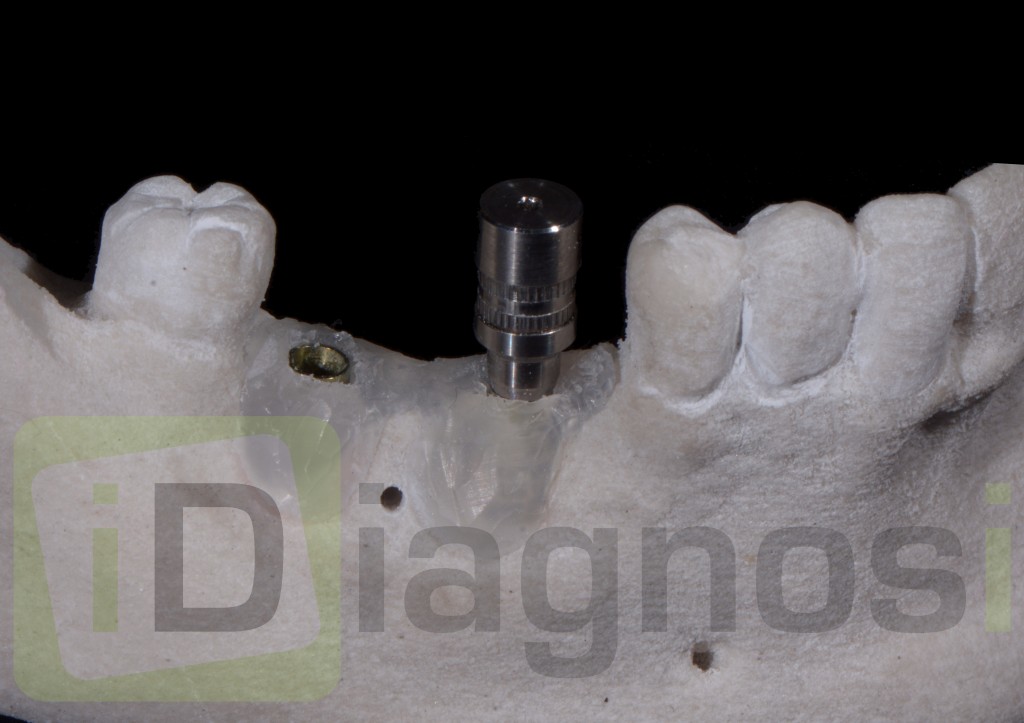
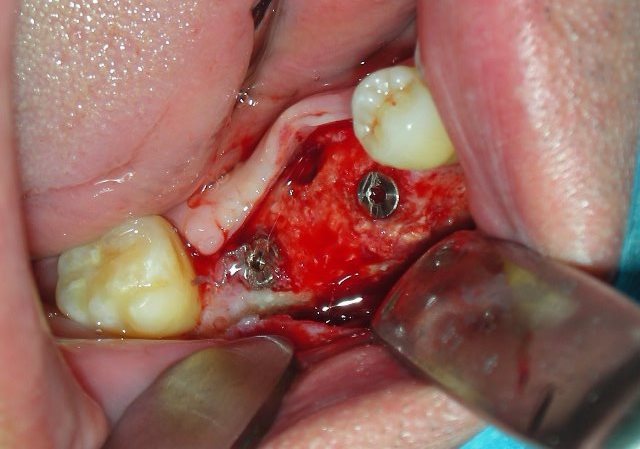
Inserimento delle coperture di guarigione.
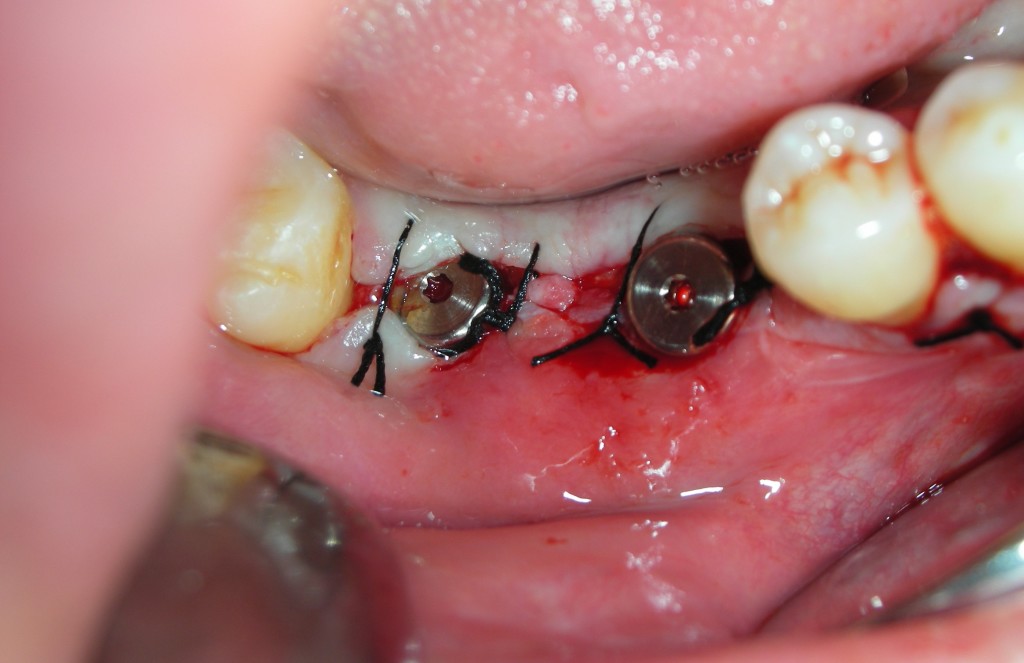
Viti di copertura e chiusura del lembo.
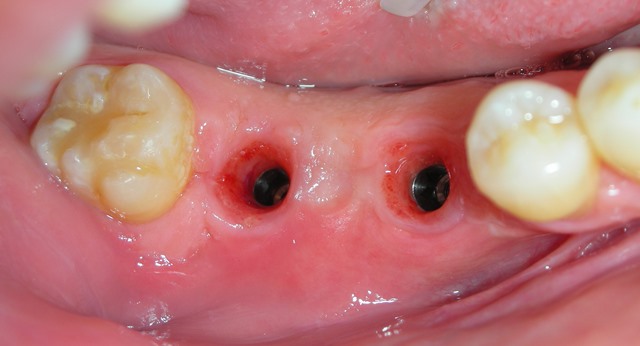
Guarigione perimetrale mucogengivale.
Inserimento abutment personalizzati.
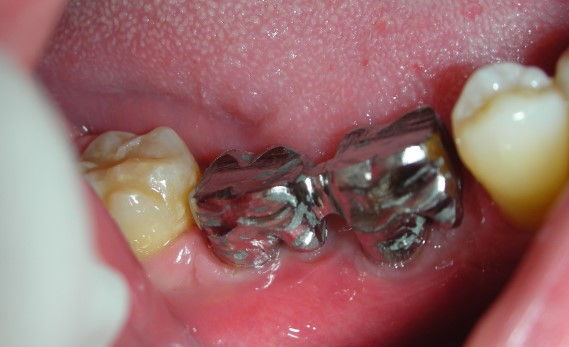
Prova della struttura.
segue….
Letture consigliate:
- Fouad Khoury. innesti ossei in implantologia, quinteessenza ed.
- Carl E. Misch. implantologia contemporanea, Elsevier ed.
- M.merli vol. 1 Terapia implantare,
- Carlo Tinti S. Parma Benfenati, GBR Rigenerazione ossea guidata a scopo implantare, ED. Nike.
Articoli correlati:
1: Wood M., Kern M, et al: TEn year clinic and microscopic avaluation of resin bonded restorations Quintessence Int 27: 808-807, 1996.
2: Goodacre CJ, Bernal G., et al: Clinical complication with implant and implant prostheses, Prosthet Dent 90: 121-132, 2003
3: Tonetti MS, Schmid J: Patogenesis of implant failures, periodontology 2000 3: 127-138,1994
4: Rangert B., Krogh PH, Langer B et al: Bending overload and fixture fratture: a retrospective clinical analysis, Int J Oral Maxillofac Implantn 10:326-334,1995
5: Balshi TJ, Wolfinger GJ: Two-implant supported sigle molar replacement: interdental space requirement and comparison to alternative optional, Int J Periodontics Restorative Dent 17:426-435, 1997
5. Discussione del caso attraverso il blog













































Lascia un commento